信号通路
信号通路(signal pathway,信号转导)是指通过细胞膜将胞外一些分子信号传到细胞内,细胞根据这些信号发生一系列效应的过程。信号通路的本质是对一系列效应调控方式的总结。
cGAS-STING信号通路
cGAS-STING信号通路是天然免疫系统中一条关键的“DNA感知”通路,负责识别胞质中异常存在的双链DNA(dsDNA),并触发I型干扰素和促炎细胞因子的表达,从而发挥抗病毒、抗肿瘤和免疫调节作用。
cGAS-STING信号通路主要成员
cGAS-STING 信号通路的核心成员可按“感受器 → 第二信使 → 接头蛋白 → 激酶 → 转录因子 → 效应分子”六层结构归纳如下
-
感受器(Sensor)
• cGAS(cyclic GMP-AMP synthase):细胞质 DNA 感受器,识别 >30 bp 的双链 DNA 后催化 ATP+GTP → cGAMP
-
第二信使(2nd messenger)
• cGAMP(2’3’-cGAMP):由 cGAS生成,直接结合并激活 STING。
-
接头蛋白(Adaptor)
• STING(TMEM173;Stimulator of Interferon Genes):内质网四次跨膜蛋白;cGAMP 结合后寡聚化并转位至高尔基体,形成信号平台。
-
激酶(Kinase)
• TBK1(TANK-binding kinase 1):被 STING 招募后自磷酸化(Ser172),继而磷酸化 STING 和 IRF3。
• IKKε/IKKβ:可协助激活 NF-κB 途径,放大炎症反应。
-
转录因子(Transcription factor)
• IRF3(Interferon regulatory factor 3): TBK1 磷酸化 IRF3-Ser396,导致其二聚并入核,启动 I 型干扰素基因。
• NF-κB(p65/p50):同时被TBK1/IKK 激活,驱动 TNF-α、IL-6 等促炎基因。
-
效应分子(Effectors)
• IFN-β、IFN-α(I 型干扰素)
• CXCL10、ISG15、IFIT1 等干扰素刺激基因(ISGs)
• TNF-α、IL-6 等 NF-κB 下游炎症细胞因子
补充协同或调控分子
• IFI16 / IFI204(PYHIN 家族)—可与 cGAS 协同增强 STING 激活。
• ULK1、TRIM32、RNF185 等 E3 泛素连接酶 — 介导 STING 降解与信号关闭。
cGAS-STING信号通路的激活与调控
激活过程:
1. DNA识别(0–5 min):cGAS识别并结合胞质中长度大于30 bp的非特异性dsDNA(如病毒DNA、肿瘤细胞基因组不稳定片段或微核破裂释放的DNA),cGAS 以 2:2 对称模式结合 dsDNA,形成“DNA-cGAS 平台”。结合后构象变化:催化口袋打开,ATP/GTP 底物通道暴露。
2. cGAMP合成(5–15 min):cGAS催化ATP和GTP生成cGAMP。
催化反应:2 ATP + 2 GTP → 2’3’-cGAMP(非经典 3’5’磷酸二酯键)。
3. STING激活(15–30 min):STING 胞质配体结合域(LBD)的 V147、Y167、R232 与 cGAMP 磷酸基团形成氢键网络。cGAMP结合内质网(ER)上的STING,STING 由“开放”转为“封闭”二聚体,并触发STING从内质网向高尔基体转运(30–60 min)。
4. 下游信号转导:STING招募TBK1(TANK结合激酶1)和IKK复合体(45–90 min),磷酸化IRF3(干扰素调节因子3)和NF-κB(核因子κB),促使IRF3二聚化和NF-κB入核,启动I型干扰素(IFN-α/β)和促炎细胞因子(如IL-6、TNF)的转录(60–120 min)。
终止机制(2–8 h):
STING被ULK1/ATG1磷酸化后,通过网格蛋白包被囊泡(CCV)转运至溶酶体降解,避免过度免疫反应。
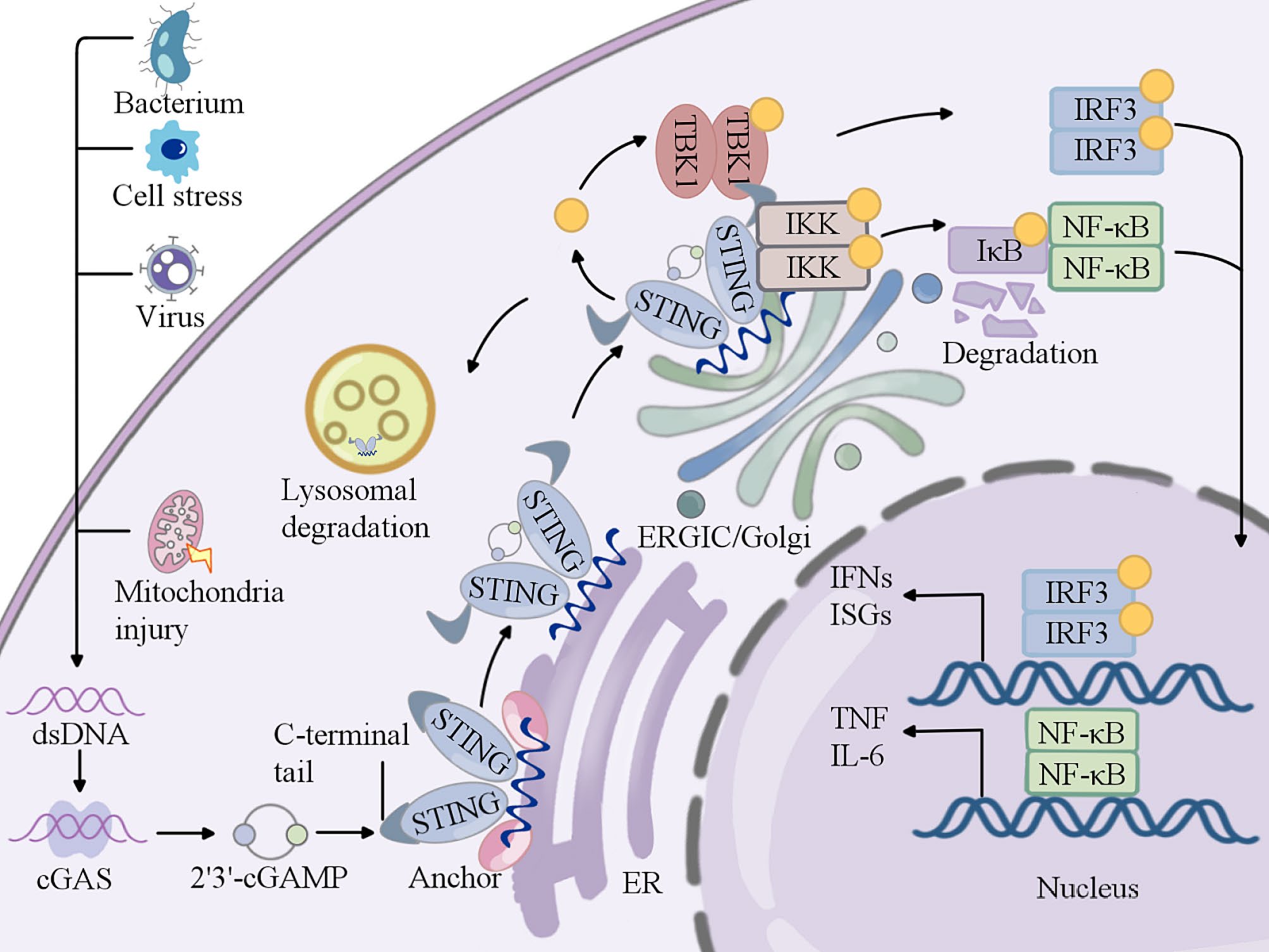
Fig. 1 Overview of the cGAS–STING pathway
图片来源:doi.org/10.1186/s12931-024-02915-x
调控机制:
1.翻译后修饰:cGAS和STING的活性受磷酸化、泛素化、SUMO化、乙酰化等多种修饰调控。例如,AKT和BLK磷酸化cGAS,RNF185介导其泛素化,而高乙酰化(如3SPF1作用)可抑制cGAS活性,用于自身免疫病治疗。
2.细胞间信号传递:在肿瘤微环境中,cGAMP、dsDNA或活化的STING可通过细胞外囊泡(如RAB22A介导的拉菲体)传递至邻近细胞,增强免疫监视。
信号通路验证
1.按时间层级验证方案总结
|
时间
|
分子事件
|
实验方法及可检指标
|
|
0–5 min
|
DNA-cGAS 结合
|
原位PLA(cGAS-DNA)
|
|
5–15 min
|
cGAMP 生成
|
LC-MS/MS cGAMP
|
|
15–30 min
|
STING 构象/棕榈酰化
|
非还原胶寡聚体
|
|
30–60 min
|
STING 转运
|
免疫荧光 ER→高尔基体
|
|
45–90 min
|
p-TBK1、p-STING
|
Western blot
|
|
1-2h
|
p-IRF3 二聚体
|
超迁移EMSA/Native-PAGE
|
|
2–8 h
|
IFN-β、ISG 表达
|
ELISA/IFN-β-Luc报告基因
|
2.WB在蛋白水平的验证方法
使用WB验证cGAS-STING 信号通路,需检测cGAS、STING(总+磷酸化)、TBK1(总+磷酸化)、IRF3(总+磷酸化) 这 6 个关键条带,再配一个阴性/抑制剂对照,即可在蛋白水平严谨判断通路是否激活。
1.cGAS(胞质DNA感受器):约60 kDa,位于胞质的单条主带。通路被激活后,其表达量可轻微上调,但更重要的是它必须与DNA结合并催化下一步反应,因此WB中常关注其总蛋白表达是否足够,而非磷酸化。
2.STING 总蛋白:约42 kDa的单体条带;在非还原胶中可见70–90 kDa的寡聚体(二聚体或高阶寡聚体)。单体总量一般不变,寡聚体出现即提示STING已发生构象变化并进入激活状态。
3.p-STING (Ser366):与总STING同一条带,但因磷酸化导致迁移略慢或条带强度明显增强。该条带的出现是STING被cGAMP激活的直接证据。
4.TBK1总蛋白:约84 kDa的单条带,总量稳定,仅作为上样对照和定位参考。
5.p-TBK1 (Ser172):同样位于84 kDa,但磷酸化后条带信号显著增强。≥2倍强度提升表示TBK1已被STING信号体招募并自激活。 IRF3总蛋白: 约55 kDa的单条带,总量不变,用于确认IRF3表达充足。
6.p-IRF3 (Ser396):55 kDa处条带增强或出现“超迁移”现象;在Native-PAGE中可见110 kDa二聚体条带。p-IRF3生成意味着TBK1已完成下游信号转导,即将启动I型干扰素基因转录。
结果解读:
激活:p-STING、p-TBK1、p-IRF3 三条磷酸化条带同步显著增强,同时非还原胶出现STING寡聚体。
阻断:上述磷酸化条带信号显著减弱或消失,提示通路被抑制。
验证案例
Li【1】等人研究cGAS-STING通路是否参与子宫内膜炎的发病机制中,验证外源性线粒体 DNA(mtDNA)是否能直接激活 cGAS-STING 通路。使用Invent 柱式法SD-001/SN-002 总蛋白提取试剂盒,从人子宫内膜基质细胞和小鼠子宫组织中提取总蛋白,WB检测 cGAS-STING 通路关键蛋白表达水平(cGAS、STING、TBK1、Pho-TBK1、IRF3、Pho-IRF3)。结果显示:mtDNA 组 vs 对照组相比,cGAS 表达上调、STING 表达升高、TBK1 和 IRF3 的磷酸化水平显著增加。说明外源性 mtDNA 能够模拟 LPS 的作用,直接激活 HESCs 中的 cGAS-STING 通路。
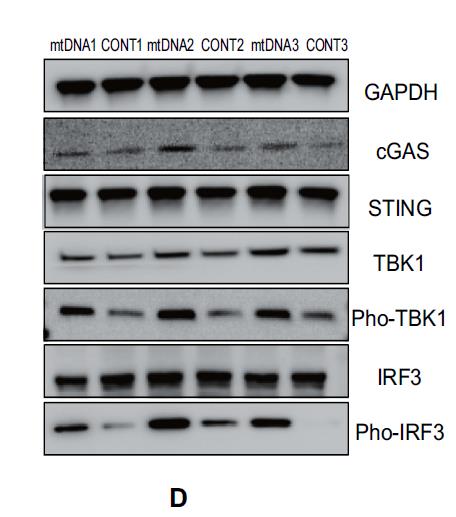
Fig2.The protein level of the cGAS-STING pathway by Western blot in indicated groups of HESCs.
图片来源:doi.org/10.2147/JIR.S374318
Liu【2】等人在研究非洲猪瘟病毒(ASFV)pB318L蛋白通过抑制 cGAS-STING 与 IFNAR-JAK-STAT 信号通路负向调控I型干扰素及干扰素刺激基因的表达实验中,为验证 ASFV 的 pB318L 蛋白是否影响STING从内质网向高尔基体的转位,使用Invent 柱式法GO-037高尔基体分离试剂盒成功从HEK293T细胞或猪肺泡巨噬细胞(PAMs)分离高尔基体组分,通过Western blot检测STING在高尔基体富集组分中的表达水平,结果表明在ASFV-WT(野生型)感染组中,STING在高尔基体上的定位显著减少;而在ASFV-intB318L(B318L缺失病毒)感染组中,STING在高尔基体上的定位明显增加。从而验证了 pB318L 蛋白影响STING从内质网向高尔基体的转位。
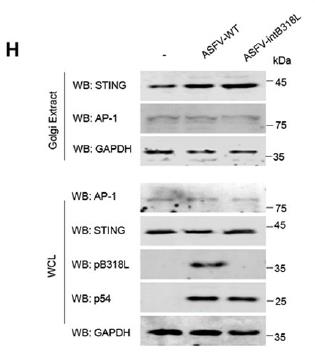
Fig3.PAMs were infected with ASFV-WT or ASFVintB318L(MOI = 1). At 24 hpi, the cells were collected and treated with Golgi Apparatus Enrichment reagent. The levels of STING on Golgi were detected by Western blotting (WCL refers to whole cell lysates)
图片来源:doi.org/10.1371/journal.ppat.1012136
参考文献
1.Li M, Wen X, Liu X, Wang Y, Yan L. LPS-Induced Activation of the cGAS-STING Pathway is Regulated by Mitochondrial Dysfunction and Mitochondrial DNA Leakage in Endometritis. J Inflamm Res. 2022;15:5707-5720 https://doi.org/10.2147/JIR.S374318
2.Liu, X., Chen, H., Ye, G., Liu, H., Feng, C., Chen, W., ... & Huang, L. (2024). African swine fever virus pB318L, a trans-geranylgeranyl-diphosphate synthase, negatively regulates cGAS-STING and IFNAR-JAK-STAT signaling pathways. PLoS pathogens, 20(4), e1012136.
3.Cui, S., Wang, Y., Chen, S., Fang, L., Jiang, Y., Pang, Z., ... & Jia, H. (2023). African swine fever virus E120R inhibited cGAS‐STING‐mediated IFN‐β and NF‐κB pathways. Animal Research and One Health.
4.Chen Wang; Xin Gao; Yanchen Li; Chenyang Li; Zhimin Ma; et al.(2024). A molecular subtyping associated with the cGAS-STING pathway provides novel perspectives on the treatment of ulcerative colitis. Scientific Reports.DOI 10.1038/s41598-024-63695-45.Kuo‐Wei Liao; Fengshuo Wang; C D Xia; Ze Xu; Sen Zhong; et al.(2024). The cGAS-STING pathway in COPD: targeting its role and therapeutic potential. Respiratory Research.DOI 10.1186/s12931-024-02915-x
6.Jia-min Du; Mei-jia Qian; Tao Yuan; Rui-han Chen; Qiao-jun He; et al.(2022).cGAS and cancer therapy: a double-edged sword.Acta pharmacologica Sinica.DOI 10.1038/s41401-021-00839-6







 站内热点
站内热点