PART01
单细胞核测序
单细胞核测序(single-nucleus sequencing,snRNA-seq)是单细胞测序的延伸技术:它不再把完整细胞送进仪器,而是把细胞核分离出来,在单个核水平完成转录组(或基因组、表观组)测序。核心目标与单细胞测序一致——捕获异质性、鉴定稀有亚群、构建细胞图谱,但样品由“抽提出的细胞核”代替“解离活细胞”,因此在很多难进行单细胞分离的样本上具有独特优势。
PART02
为什么用单细胞核测序
大脑是人体最复杂的器官之一,其功能依赖于高度多样化和特异性的大脑细胞类型。这些细胞在基因表达、形态、功能和连接方面存在显著差异,是神经学研究的重要材料。但绝大多数大脑样本来源于死后的冷冻组织,细胞膜在冷冻-解冻过程中容易破裂,很难分离出有活性的单细胞。另外如小胶质细胞等脑细胞与神经元和其他胶质细胞紧密交织,通过物理或酶学方法分离单细胞时会强烈激活它们,改变其基因表达,引入实验误差。
而细胞核膜更为坚韧,在冷冻条件下更易保持完整,且分离细胞核是一个相对温和的过程,能更好地保留细胞在体内的原始转录状态。因此单细胞核RNA测序(snRNA-seq)技术的出现,为神经科学领域带来了革命性的变化。使得对珍贵的冷冻脑组织、尸检脑组织、固定临床病理标本以及复杂神经网络进行精细的细胞分型和状态分析成为可能。
PART03
snRNA-seq如何驱动神经科学新发现
凭借其独特优势,snRNA-seq正在多个神经学前沿领域催生突破性进展:
癫痫:癫痫是一种常见的神经系统疾病,其发病机制涉及大脑神经元的异常放电。研究者利用snRNA-seq,在局灶性皮质发育不良患者脑组织中,精准鉴定出新的嵌合MTOR变异,为理解疾病遗传基础提供了关键线索【1】。
疼痛:疼痛的感知和调节涉及大脑中多个脑区和细胞类型。通过解析疼痛相关脑区的细胞图谱,科学家发现了一条全新的伤害性杏仁核-纹状体通路,为开发非阿片类镇痛药提供了潜在靶点【2】。
睡眠:睡眠是大脑的重要功能之一,其调节机制复杂且涉及多种细胞类型。在小鼠模型中,snRNA-seq成功识别出在睡眠剥夺恢复期间被特异性激活的甘丙肽神经元亚型,揭示了睡眠调节的崭新细胞基础【3】。
阿尔茨海默病:阿尔茨海默病等神经退行性疾病的发病机制与大脑中特定细胞类型的功能障碍密切相关。snRNA-seq结合多基因风险评分,揭示了阿尔茨海默病中存在的不同小胶质细胞病理亚型,为未来的精准分型与治疗奠定了基础【4】。
大脑发育:大脑发育过程中,神经干细胞的分化和迁移受到精确的基因调控。研究通过snRNA-seq证实了小鼠杏仁体发育的新放射状迁移模型,深化了我们对大脑这一神秘区域细胞起源的认识【5】。
PART04
snRNA-seq的核心技术流程
snRNA-seq在神经科学研究中的通用流程可概括为以下四个关键环节:
1. 样本准备与核分离
样本来源:主要采用快速冷冻的脑组织(动物或人)、术中新鲜获取的活体人脑组织(如癫痫手术样本)或存档的冰冻组织。样本质量是决定数据可靠性的基础。
核分离:通过机械匀浆结合非离子去污剂(如专用细胞核分离试剂盒或自配缓冲液),温和裂解细胞膜,释放完整细胞核,并确保核膜完整性以最大限度减少RNA泄漏。
2. 单核RNA文库构建与测序
将纯化后的细胞核加载至微流控平台(如10x Genomics),使其与带有细胞条形码和UMI的磁珠共同包裹于油滴内,形成GEM;
在油滴内完成逆转录,生成带细胞标签的cDNA;
破碎油滴并扩增cDNA,构建适用于下一代测序的文库;
使用Illumina等高通量测序平台进行测序。
3. 生物信息学分析
数据质控与比对:借助Cell Ranger等工具将原始测序数据比对至参考基因组,完成细胞条形码计数与质控;
细胞聚类与注释:利用Seurat或Scanpy进行降维(PCA、UMAP)与无监督聚类,再依据已知标记基因(如SNAP25–神经元、GFAP–星形胶质细胞、MOBP–少突胶质细胞、P2RY12–小胶质细胞)鉴定细胞类型;
差异分析与功能挖掘:比较不同实验条件下特定细胞类型的基因表达差异,开展基因集富集分析,识别相关通路变化;
高级分析:可进一步进行细胞轨迹推断(拟时间分析)、细胞–细胞通讯分析、或与基因组数据整合,以揭示更深层生物学机制。
4. 实验验证
关键发现需通过独立实验进行验证,常用方法包括:
RNAscope/原位杂交:在组织原位验证基因的细胞类型特异性表达;
免疫组化/免疫荧光:确认目标蛋白的表达与定位;
功能实验:如光遗传学、化学遗传学或行为学测试,以阐明特定细胞亚群的功能作用。
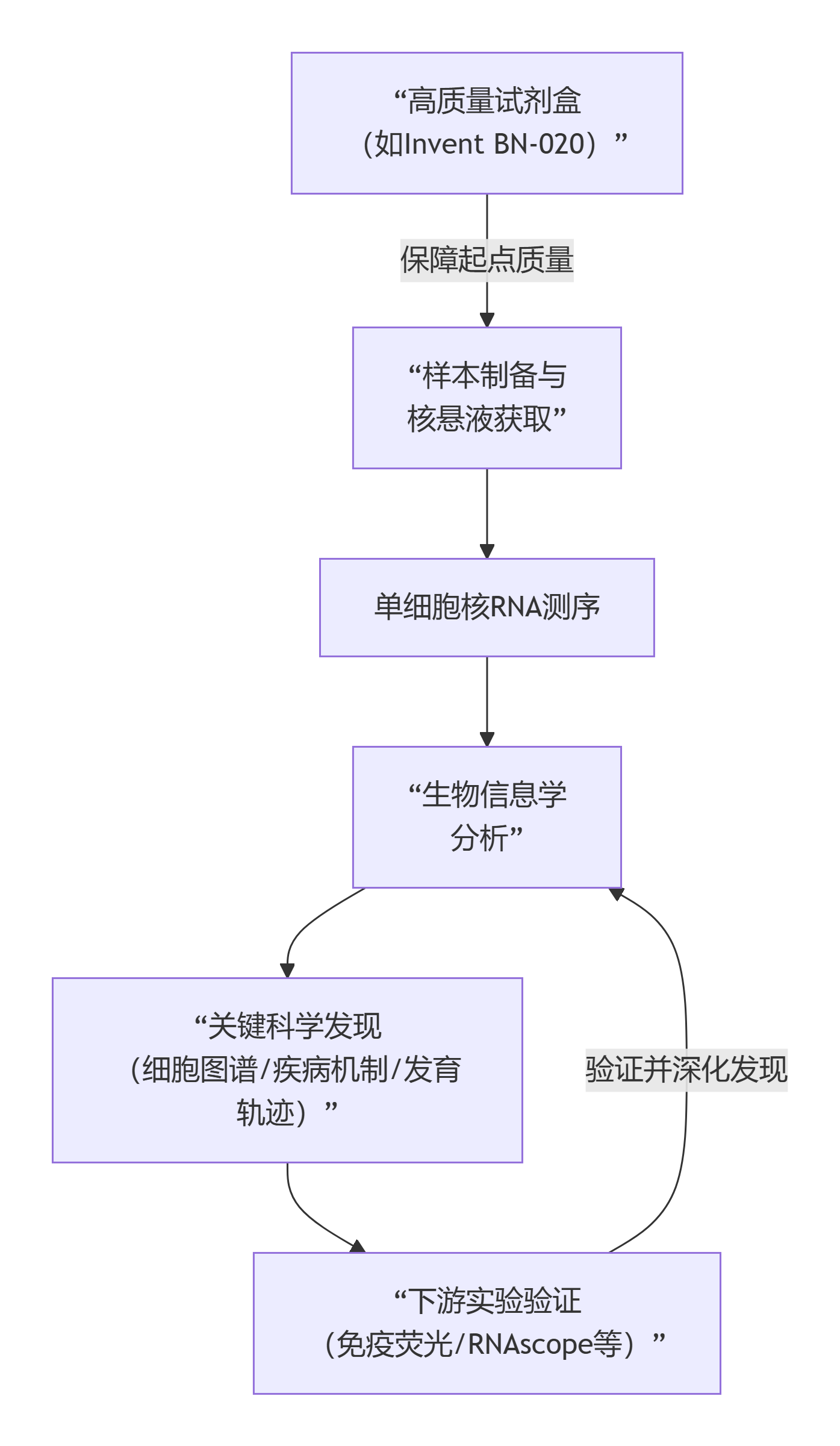
Fig.snRNA-seq的核心技术流程
PART05
成功之钥:分离高质量细胞核
单细胞核测序的第一步——获得高质量、完整无降解的单个细胞核悬液,是整个项目成败的生命线。尤其是对于脂质含量高、细胞连接复杂的大脑组织,通用的提取方法往往效果不佳。
专业化解决方案:针对神经组织优化的商业化核分离试剂盒(Invent Minute™ 神经元组织/细胞单个细胞核分离试剂盒 BN-020 点击查看),提供了标准化、可重复的解决方案。
确保数据真实可靠:其优化的裂解体系能有效处理髓鞘等复杂结构,在释放各类细胞核的同时,最大程度防止RNA降解,这对于准确捕获稀有细胞亚群(如研究中发现的特定神经元)的转录状态至关重要。
赋能珍贵样本研究:对于不可复得的人脑尸检、临床手术样本,一个可靠高效的核分离工具,是连接宝贵生物学样本与高质量基因组数据之间不可或缺的桥梁,直接推动了人类神经科学的进步。
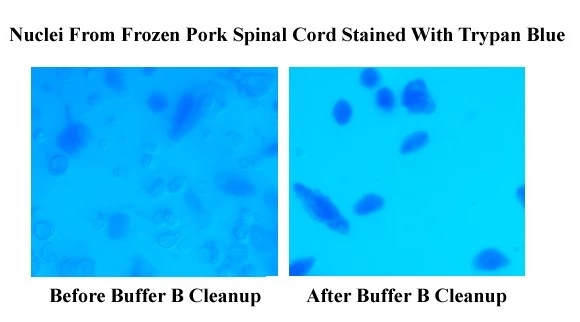
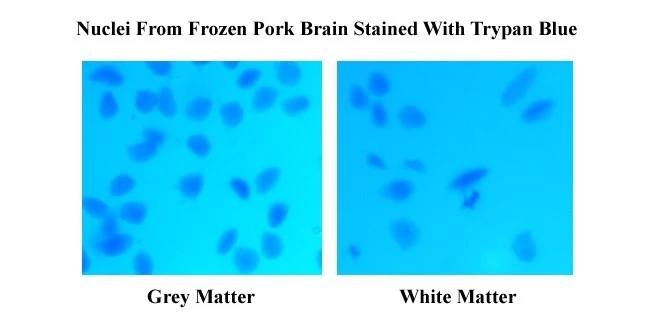
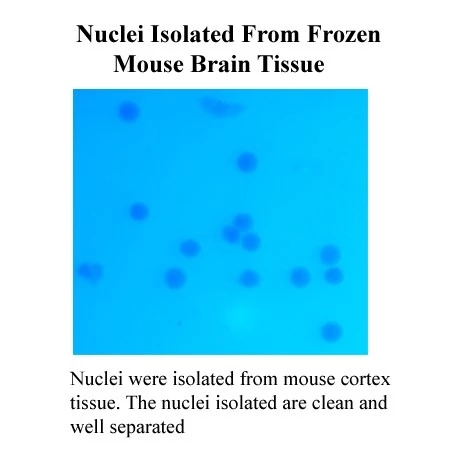
BN-020效果图
PART06
结论
单细胞核RNA测序技术以其卓越的解析力,为我们揭开了大脑在发育、功能、疾病与衰老过程中潜藏的分子图景。这一技术不仅重塑了我们对神经系统的认知框架,更推动了神经科学迈入精准化与系统化的新阶段。而稳定高效的细胞核分离方案,如Invent BN-020,作为连接生物样本与多维组学数据的关键桥梁,为探索大脑奥秘提供了坚实的技术基石。单细胞核测序,正以其前所未有的分辨率,成为驱动神经科学从观察到干预、从理解到重塑的核心引擎。
扫码与我交流
PART07
参考文献
1.Klein, K. M., Mascarenhas, R., Merrikh, D., Khanbabaei, M., Maroilley, T., Kaur, N., ... & Tarailo-Graovac, M. (2024). Identification of a novel mosaic MTOR variant in purified neuronal DNA from depth electrodes in a patient with focal cortical dysplasia. Epilepsia, 2024-06.
2. Jessica A. Wojick; Alekh Paranjapye; Juliann K. Chiu; Corinna S. Oswell; Malaika Mahmood; et al (2025). A nociceptive amygdala-striatal pathway modulating affective-motivational pain. Science Advances, DOI 10.1126/sciadv.ado2837
3.Guo, X., Keenan, B. T., Reiner, B. C., Lian, J., & Pack, A. I. (2024). Single-nucleus RNA-seq identifies one galanin neuronal subtype in mouse preoptic hypothalamus activated during recovery from sleep deprivation. Cell Reports, 43(5).
4.Masataka Kikuchi; Akinori Miyashita; Yu Hirota; Norikazu Hara; Mai Hasegawa;et.al.(2025).Microglia-specific polygenic risk stratification reveals distinct pathological subtypes in Alzheimer’s disease.medRxiv.DOI 10.1101/2025.10.06.25336925
5.Fernández, G.;López-González, L.; Pons-Fuster, E.;Puelles, L.; Garcia-Calero, E.(2025).Transcriptomic Analysis Corroborates the New Radial Model of the Mouse Pallial Amygdala. Biomolecules 2025,15, 1160. https://doi.org/10.3390/biom15081160
6.Kalef-Ezra, E., Friscioni, L., Horner, D., Morley, C., Morrow, G., Guo, Y., & Proukakis, C. (2024). Fluorescence-activated nuclei sorting (FANS) for single-cell Whole Genome Sequencing (scWGS).
7.James, J. G., McCall, N. M., Hsu, A. I., Oswell, C. S., Salimando, G. J., Mahmood, M., ... & Corder, G. (2024). Mimicking opioid analgesia in cortical pain circuits. bioRxiv, 2024-04.
8.Vornholt, E., Liharska, L. E., Cheng, E., Hashemi, A., Park, Y. J., Ziafat, K., ... & Beckmann, N. D. (2024). Characterizing cell type specific transcriptional differences between the living and postmortem human brain. medRxiv, 2024-05.
9.Rodriguez de los Santos, M., Kopell, B. H., Buxbaum Grice, A., Ganesh, G., Yang, A., Amini, P., ... & Breen, M. S. (2024). Divergent landscapes of A-to-I editing in postmortem and living human brain. Nature Communications, 2024-05.
10.Tyshkovskiy, A., Kholdina, D., Ying, K., Davitadze, M., Molière, A., Tongu, Y., ... & Gladyshev, V. N. (2024). Transcriptomic Hallmarks of Mortality Reveal Universal and Specific Mechanisms of Aging, Chronic Disease, and Rejuvenation. bioRxiv, 2024-07.
11.Mascarenhas, R., Merrikh, D., Khanbabaei, M., Kaur, N., Ghaderi, N., Maroilley, T., ... & Klein, K. M. (2024). Detecting somatic variants in purified brain DNA obtained from surgically implanted depth electrodes in epilepsy. medRxiv, 2024-07.
12.Rodrigues-Amorim, D., Bozzelli, P. L., Kim, T., Liu, L., Gibson, O., Yang, C. Y., ... & Tsai, L. H. (2024). Multisensory gamma stimulation mitigates the effects of demyelination induced by cuprizone in male mice. Nature Communications, 15(1), 6744.
13.McSwiggin, H., Wang, R., Magalhaes, R. D. M., Zhu, F., Doherty, T. A., Yan, W., & Jendzjowsky, N. (2024). Comprehensive sequencing of the lung neuroimmune landscape in response to asthmatic induction. bioRxiv, 2024-10.
14.Brian H. Kopell; Deepak Kaji; Lora E. Liharska; Eric Vornholt; Alissa Valentine; et al.(2024).Multiomic foundations of human prefrontal cortex tissue function.medRxiv (Cold Spring Harbor Laboratory).DOI 10.1101/2024.05.17.24307537
15.Hashimoto S, Nagoshi N, Shinozaki M, Nakanishi K, Suematsu Y, Shibata T, Kawai M, Kitagawa T, Ago K, Kamata Y, Yasutake K, Koya I, Ando Y, Minoda A, Shindo T, Shibata S, Matsumoto M, Nakamura M, Okano H. Microenvironmental modulation in tandem with human stem cell transplantation enhances functional recovery after chronic complete spinal cord injury. Biomaterials. 2023 Apr;295:122002. doi: 10.1016/j.biomaterials.2023.122002. Epub 2023 Jan 26. PMID: 36736008.
16.Blake A. Kimmey; Lindsay L. Ejoh; Lily Shangloo; Jessica A. Wojick; Samar N. Chehimi; et al.(2025).Convergent state-control of endogenous opioid analgesia.bioRxiv.DOI 10.1101/2025.01.03.631111
17.Nicha Puangmalai; Abbigael E Aday; Madison Samples; Nemil Bhatt; Filippa Lo Cascio; et al.(2025).Pathogenic Oligomeric Tau alters Neuronal RNA Processes through the Formation of Nuclear Heteromeric Amyloids with RNA-Binding Protein Musashi1.Progress in Neurobiology.DOI 10.1016/j.pneurobio.2025.102742
18. Anika Nabila; Rose Sciortino; Nicole Politowska; Elizabeth Brindley; Peter U. Hámor; et al.(2025).Adverse gestational environment configures a subpopulation of ventral dentate granule cells for recruitment to drive innate anxiety.Cell Reports.DOI 10.1016/j.celrep.2025.116219
19.McSwiggin H, Wang R, Magalhães RDM,Zhu F, Doherty TA, Yan W and Jendzjowsky N.(2025) Comprehensive sequencing of the lung neuroimmune landscape in response to asthmatic induction.Front. Immunol. 16:1518771.doi: 10.3389/fimmu.2025.1518771







 站内热点
站内热点